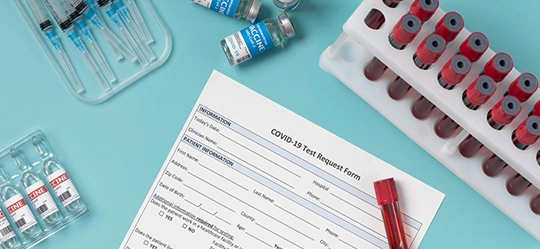
Ein Biotech-Unternehmen plante den Start einer klinischen Phase-III-Studie für ein vielversprechendes, neues Krebsmittel. Die Durchführung der Studie war in 16 Ländern geplant, darunter die Vereinigten Staaten, Deutschland, Japan, China usw. In jedem dieser Märkte gelten strenge und unterschiedliche Compliance-Anforderungen in Bezug auf die Kennzeichnung von Prüfpräparaten (IMPs).
Im Zuge der Studie galt es sicherzustellen, dass die IMP-Kennzeichnungen die unterschiedlichen und komplexen Vorschriften des jeweiligen Landes einhalten, da eine Nichteinhaltung die Studie verzögern, Geldstrafen nach sich ziehen oder die Studienergebnisse ungültig machen und sich negativ auf die Inverkehrbringung und den Erfolg des Medikaments auswirken würde.
Die Zielvorgabe war somit die Durchführung einer umfassenden Compliance-Überprüfung der geplanten IMP-Kennzeichnungen, um die vollständige Einhaltung der FDA-, EMA- und PMDA-Vorschriften und den reibungslosen Start der globalen klinischen Studie zu gewährleisten.
Entwicklung einer Compliance-Strategie: Zusammen mit dem Kunden erarbeitete unser Team die spezifischen Anforderungen für die klinische Studie und formulierte eine maßgeschneiderte Compliance-Strategie für die IMP-Kennzeichnungen.
Überprüfung von Dokumenten und Compliance-Beurteilung: Die ersten Kennzeichnungsentwürfe wurden im Detail überprüft und mit den aktuellen Compliance-Richtlinien der FDA, EMA und PMDA verglichen. Sämtliche am Projekt beteiligten Fachexperten waren Manager mit mehr als sieben Jahren Erfahrung in den Bereichen Compliance-Richtlinien und Übersetzung.
Überprüfung und Lokalisierung der Kennzeichnungen: Basierend auf den gewonnenen Erkenntnissen empfahlen wir bestimmte Änderungen am Wortlaut, Layout und in Bezug auf die Übersetzungsanforderungen. So stellten wir sicher, dass alle Kennzeichnungen die örtlichen Vorschriften erfüllten und trotzdem in den verschiedenen Regionen konsistent waren.
Abschließende Prüfung und Abnahme: Nach der Überarbeitung führten wir eine abschließende Compliance-Prüfung durch, bevor die Kennzeichnungen gedruckt und an den Prüfpräparaten angebracht wurden.
Erfolgreiche Einhaltung der Vorschriften: Alle IMP-Kennzeichnungen wurden von den jeweiligen Zulassungsbehörden ohne weitere Änderungen genehmigt.
Fristgerechter Start der Studie: Die klinische Studie konnte in allen Regionen planmäßig und ohne kostspielige Verzögerungen gestartet werden.
Risikominderung: Potenzielle rechtliche und finanzielle Risiken einer Nichteinhaltung wurden erfolgreich reduziert.
Das Fallbeispiel zeigt die zentrale Rolle, die eine fachkundige Compliance-Überprüfung bei der erfolgreichen Durchführung internationaler klinischer Studien spielt. Wir stellten sicher, dass die IMP-Kennzeichnungen die regionalen Vorschriften einhielten, sodass das Produkt des Unternehmens die rechtlichen Anforderungen erfüllte und die Studie durchgeführt werden konnte.

 EN
EN  cn
cn  de
de  jp
jp